Wyniki pomiarów fizykochemicznych to często jedne z podstawowych informacji istotnych dla automatyków czy technologów. Stężenie substancji, pH, barwa, ilość tlenu – dostęp do tych i wielu innych danych decyduje nierzadko o efektywności prowadzonych procesów. Wyjaśnijmy więc, co kryje się po tym pojęciami i jakie zasady wykorzystują urządzenia pomiarowe.
Pomiar pH
Jak wiadomo, wartość pH określa kwasowość bądź zasadowość roztworu. Roztwory obojętne posiadają pH równe 7 (czysta woda), powyżej pH 7 mamy do czynienia z zasadami (do pH 14), poniżej – z kwasami (do pH=0). Pojęcie pH wprowadził duński biochemik Søren Sørensen w roku 1909. Jego definicja określała pH jako ujemny logarytm ze stężenia jonów wodorowych:
![]()
Z czasem okazało się, że wolne jony wodorowe (H+) – wolne protony – nie występują w roztworach wodnych, ponieważ natychmiast ulegają solwatowaniu:
![]()
Definicja została zmieniona i obecnie mówi ona, że pH jest to ujemny logarytm aktywności jonów hydroniowych w molach na decymetr sześcienny:
![]()
Dziś pH jest mierzone metodami galwanometrycznymi.
Najbardziej poprawnie określa tę wartość norma ISO i Unia Chemii Czystej i Stosowanej, stosując następujący wzór:
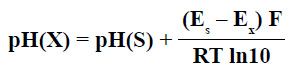
gdzie F to stała Faradaya, R uniwersalna stała gazowa, T temperatura w skali Kelvina a Es i pH(S) siła elektromagnetyczna ogniwa standardowego.
Ze wzoru wynika, że pH jest wielkością bezwymiarową i porównawczą, bez odwoływania się do aktywności jonów hydroniowych. Pierwotnie skala pH została zdefiniowana dla rozcieńczonych roztworów kwasów, zasad i soli. W takim przypadku pH mieści się w przedziale 0-14. Odnośnie roztworów stężonych, w których działają inne mechanizmy, pH może wykraczać poza tradycyjny zakres tak w dół jak i w górę (np. -2 lub + 16).
Przewodność roztworów
Aby roztwór przewodził prąd elektryczny, muszą się w nim znajdować substancje, które uległy dysocjacji, czyli rozpadowi na jony. Taki roztwór nazywamy elektrolitem, a przewodzenie prądu jest efektem migracji znajdujących się w nim jonów.
Jednostką podstawową przewodności w układzie SI jest S/m (simens/metr). W praktyce posługujemy się przeważnie jednostkami podrzędnymi μS/cm lub mS/cm. Jednym ze sposobów pomiaru przewodności jest metoda konduktancyjna. Czujnik stanowi naczyńko konduktometryczne, wyposażone w dwie elektrody, których wzajemna odległość jest określana jako stała K. Im roztwór zawiera mniej zdysocjowanych substancji, tym stała K musi być mniejsza (i odwrotnie, im więcej substancji rozpuszczonej, tym większa stała K). Prąd płynący między elektrodami określa przewodność roztworu.
Ten rodzaj pomiaru może być stosowany do roztworów niezabrudzonych, bez zawiesiny i wtrąceń stałych. W przypadku cieczy i roztworów brudnych (np. ścieków), stosuje się pomiar metodą indukcyjną. Czujnik indukcyjny składa się z dwóch cewek. Zasilana prądem cewka pierwotna wytwarza w cieczy pole elektromagnetyczne, indukujące prąd w cewce wtórnej. Przy stałej wartości zasilania, natężenie powstałego pola elektromagnetycznego, a więc i wielkość indukowanego prądu, jest proporcjonalna do ilości jonów w roztworze.
Praktycznie w każdej, najczystszej nawet wodzie, znajdują się niewielkie ilości zdysocjowanych substancji. Np. woda pitna ma przewodność 0,5 – 1 mS/cm, woda w czystym, górskim potoku ok. 10 μS/cm, woda destylowana ok. 0,5 μS/cm a woda kotłowa od 0,05 do 1 μS/cm.
Pomiar tlenu rozpuszczonego
Tlen rozpuszczony w wodzie stanowi warunek konieczny życia wielu organizmów. Zarówno w wodach otwartych (jeziorach, rzekach) jak i w różnych zbiornikach (w oczyszczalniach ścieków, stawach rybnych), obecność tlenu jest niezbędna. Z drugiej strony istnieją miejsca, gdzie rozpuszczony tlen jest elementem szkodliwym. Tak jest np. w przypadku wody kotłowej. W każdej sytuacji zawartość tlenu trzeba zmierzyć. Znanym od dawna rodzajem pomiaru jest metoda polarograficzna. Zasada polega na pomiarze prądu elektrycznego, płynącego w ogniwie pomiarowym, proporcjonalnego do zawartości tlenu.
Podstawowym elementem czujnika jest komora wyposażona w półprzepuszczalną membranę; wewnątrz której znajdują się dwie elektrody i elektrolit. Membrana nie stanowi przeszkody dla rozpuszczonego tlenu, jest natomiast nieprzepuszczalna dla wody, w której jest zanurzony czujnik. Membrana to przeważnie błonka z teflonu o grubości ok. 50 μm. Molekuły tlenu swobodnie dostają się do środka komory w ilości odpowiadającej ich stężeniu w roztworze.
Do elektrod wewnątrz komory przykładane jest stałe napięcie polaryzacyjne. Przenikający przez membranę tlen, dyfundując przez elektrolit, jest redukowany na katodzie. Generowany prąd jest przeliczany na zawartość tlenu. Nowatorskim pomysłem, górującym nad dotychczasowymi sposobami pomiaru jest metoda luminescencyjna. W pomiarze wykorzystuje się zjawisko luminescencji, czyli zdolności niektórych substancji (luminoforów) do emisji światła pod wpływem dostarczonej energii (też w postaci światła o innej długości fali). Mówiąc prościej, luminofor, po oświetleniu światłem o odpowiednio dobranej barwie (czyli o odpowiedniej długości fali elektromagnetycznej), zaczyna sam świecić ale światłem o innej barwie.
Głównymi elementami czujnika są:
- dioda niebieska pobudzająca luminofor,
- dioda czerwona spełniająca zadanie kontrolne i diagnostyczne oraz fotodetektor mierzący czas trwania luminescencji.
Światło błysku diody niebieskiej powoduje wzbudzenie luminoforu, który zaczyna świecić światłem czerwonym. Czas świecenia jest zależny od stężenia tlenu. Jest to zależność odwrotnie proporcjonalna; im więcej tlenu rozpuszczonego, tym krótszy czas luminescencji i na odwrót. Dioda czerwona, błyskająca pomiędzy rozbłyskami diody niebieskiej, kontroluje poprawność pracy układu. Metoda jest bardzo precyzyjna i pozbawiona wad wcześniej wymienionego sposobu pomiaru. Nie wymaga ruchu cieczy (przepływu), jest odporna na obecność siarkowodoru (częstego składnika ścieków), nie wymaga okresowej kalibracji.
Twardość wody
Twardość wody jest miarą zawartości soli wapnia, magnezu (kationów podstawowych) oraz jonów żelaza, glinu, manganu i metali ciężkich (arsenu, ołowiu, niklu, chromu). Ogólna twardość wody jest sumą twardości przemijającej i trwałej. Twardość przemijająca (zwana także węglanową) powodowana jest przez węglany (sole kwasu węglowego). Twardość trwała jest efektem zawartości soli innych kwasów: chlorków, siarczanów, azotanów.

Fotometryczny pomiar barwy i mętności
Twardość wody wpływa na jej napięcie powierzchniowe, czego zauważalnym efektem jest trudność w zwilżaniu powierzchni, a więc problem z myciem i praniem. Zastosowanie detergentów zmniejsza twardość wody, ułatwiając jej użycie do celów higienicznych. W przemyśle problem jest znacznie poważniejszy. Twardość przemijająca jest przyczyną osadzania się kamienia kotłowego, co prowadzi do niebezpiecznych i kosztownych awarii. Z tego względu, w przemyśle stosuje się różne metody zmiękczania i demineralizacji wody. Jedne sprowadzają się do dodawania substancji chemicznych (wapna, kwaśnego węglanu sodu, wodorotlenku sodu, fosforanu sodu), inne polegają na przepuszczaniu wody przez kolumny jonitowe (wymieniacze jonowe) – w kolumnach następuje wymiana kationów czyli powstają inne, niegroźne związki.
Twardość wody jest oznaczana metodą laboratoryjną. Do tego celu wykorzystuje się kwas wersenowy, powszechnie znany jako EDTA (skrót jego angielskiej nazwy), a właściwie jego sól, wersenian dwusodowy. Substancja ta ma własność tworzenia barwnych tzw. kompleksów, związków z kationami takich metali jak wapń, magnez lub żelazo. Próbkę wody miareczkuje się mianowanym roztworem wersenianu do zmiany barwy. Z ilości zużytego wersenianu wylicza się twardość wody, stosując różne jednostki. Najpopularniejsze to: stopnie niemieckie (°dH), stopnie francuskie (°f) a także mval/l (milival/l), często stosowane w Polsce. Zależność między tymi jednostkami jest następująca:
1 mval/l = 5 °f = 2,8 °dH.
Pomiary laboratoryjne z powodzeniem może zastąpić prosty i niedrogi automatyczny analizator twardości wody. Urządzenie wykorzystuje metodę laboratoryjną. Próbka wody wypełniająca komorę pomiarową, jest miareczkowana roztworem wersenianu podawanym małymi porcjami pompką perystaltyczną z pojemnika, z ciągłym mieszaniem. Koniec miareczkowania (zmianę barwy roztworu) określa fotometr. Zużycie odczynnika wyliczane jest z ilości obrotów pompki perystaltycznej. Elektronika przelicza ilość zużytego wersenianu na twardość wody. Urządzenie jest programowalne i w pełni bezobsługowe (wymaga jedynie dostarczania pojemnika z roztworem wersenianu, średnio raz na trzy miesiące).
Pomiar mętności i barwy
Pomiar mętności polega na określeniu natężenia światła promieni, odchylonych przez cząstki zawieszone w cieczy. Ciecz przepływająca przez komorę pomiarową, prześwietlana jest strumieniem światła. Po drugiej stronie komory znajdują się promieniście usytuowane detektory, wyłapujące promienie, które zmieniły tor na skutek odbicia się od cząsteczek zawartych w przepływającej cieczy. Im więcej cząsteczek w cieczy, tym więcej promieni trafiających do detektorów. Pomiar wykorzystywany jest do kontroli klarowności produktów (piwo!) oraz sprawności filtrów. Pomiar barwy ma nieco inną zasadę. Wykorzystuje się w nim prawo Lamberta-Beera. Prawo to mówi, że spadek natężenia światła przechodzącego przez ciecz, jest proporcjonalny do stężenia substancji zawartej w tej cieczy. Innymi słowy, im bardziej intensywna barwa roztworu, tym większa różnica między natężeniem światła wchodzącego i wychodzącego. Oczywiście kluczową sprawą jest dobór właściwej dla danego pomiaru (barwy) długości fali świetlnej i tzw. długości drogi optycznej.
Pomiar stężenia roztworów
Pomiar stężenia roztworów jest ważny a jednocześnie – wbrew pozorom – niezbyt łatwy. Wyróżniającą się metodą jest pomiar współczynnika załamania światła roztworu. Zasada pomiaru wykorzystuje sposób zachowania się promieni świetlnych, padających na granicę dwóch ośrodków, z których jednym jest mierzony roztwór, a drugim „szkiełko” przyrządu pomiarowego (faktycznie jest to syntetyczny diament). Na granicy tych ośrodków, promienie odbijają się całkowicie bądź częściowo. Obrazy jakie na zespole fotodetektorów dają te odbicia, oddzielone są ostrą granicą umożliwiającą (po odpowiedniej obróbce sygnałów przez elektronikę i przeliczeniu) pomiar stężenia z dokładnością 0,1% (lub 0,1°Brix) w całym zakresie od 0 do 100%. Najważniejszymi zaletami tej metody są: kompletna niewrażliwość na stałe wtrącenia bądź zanieczyszczenia roztworu (kryształki, zaśmiecenia, pęcherzyki gazów, zmiana barwy) oraz brak dryftu kalibracji (co skutkuje zbędnością kalibracji przez cały okres użytkowania).
Urządzeniami wykorzystującymi tę metodę są refraktometry procesowe.
Powyższa lista pomiarów fizykochemicznych nie jest oczywiście kompletna. W przemyśle wykorzystuje się jeszcze wiele innych pomiarów z tej dziedziny. Te wymienione w artykule są jednak stosunkowo najpopularniejsze.